Аэрация воды из скважины: принципы обезжелезивания. Очистка воды от кислорода
Очистка воды кислородом, как это происходит?
Очистка воды кислородом или аэрация – важный процесс, который лежит в основе операции по очищению питьевой воды. Он используется для обеспечения стабильной циркуляции воды в бассейнах, недопущения цветения водоемов, очищения стоков.
Очистка питьевой воды кислородом – эффективный метод удаления вредных для здоровья человека химических соединений. В состав неочищенной воды могут входить вещества, способные воздействовать на человека негативно. К ним относятся сероводород, гидроокись железа, диоксид углерода и другие вредные вещества. Водоочистка кислородом позволяет удалить подобные вещества за счет проведения химической реакции с кислородом и, так называемого, продувания летучих токсичных соединений. Очистка воды для питья кислородом в системах аэрации нужна в виду лишения воды кислорода из глубоких скважин.
Для удаления растворенных металлов, сероводорода, органических загрязнений, летучих соединений из воды необходимо сначала эти примеси окислить. Обработка окислителями – это одна из основных стадий очистки воды. Для окисления примесей, содержащихся в воде – ионов железа, марганца, алюминия, растворенных газов и органических соединений - применяются различные методы. Можно использовать, хлор, озон, гипохлориты, перекись водорода или перманганат калия. Самый доступный и экологический окислитель – кислород. В напорную водопроводную магистраль подается кислород при помощи аэрационного эжектора или компрессора для аэрации воды.
Очистка воды кислородом может быть двух видов. Это безнапорная аэрация и напорная аэрация.
Напорная аэрация воды. Процедура окисления кислородом растворенных в воде металлов довольно длительная в сравнении с химическими методами окисления. Аэрационная колонна играет роль контактной камеры. Воздушная смесь вводится внутрь колонны через ее оголовок по падающей трубе. Интенсивное окисление примесей за счет барботирования воды всплывающими пузырьками воздуха в толще водяного слоя. Кроме окислительных реакций при водоподготовке происходит удаление из воды растворенных газов и излишнего воздуха.
Воздухоотводящий клапан, находящийся в верхней части аэрационной колонны выпускает излишки воздуха и газы, которые накапливаются в верхней части колонны. Рабочий процесс клапана основан на закрытии или открытии глубоким уплотнителем выходного отверстия при всплытии или опускании поплавка. При нахождении кислорода под поплавком, он свободно проходит наружу через имеющие выходные каналы. Когда выпущен весь кислород, и появляется вода под поплавком, поплавок всплывает, и гибкий уплотнитель перекрывает выходное отверстие.
Аэрационную колонну вода наполняет не полностью. На границе воды и воздуха проходит вторичная очистка воды для дома кислородом.
Вода, насыщенная кислородом, с окислительными примесями по коллектору выводится из колонны.
В некоторых случаях применяется очистка воды кислородом упрощенная. Преимущество такой очистки заключается в ее низкой стоимости в виду отсутствия колонны. Использование подобной технологии очистки воды кислородом имеет некоторые ограничения.
Безнапорная аэрация воды. С растворенными примесями вода поступает в окислительный бак, где и происходит ее распыление. Дополнительная очистка воды кислородом осуществляется при помощи форсунок душирования или безнапорного аэрационного эжектора. Вода в окислительном баке перемешивается, это значительно ускоряет процедуру окисления железа и газов.
Так как происходит разрыв струи в безнапорной аэрационной станции, то после нее необходимо устанавливать насосную станцию для того, чтобы поднимать давление до нужной величины. Постепенно на дне окислительного бака скапливается слой окислившегося железа, который с периодичностью в два или четыре раза в год необходимо удалять. Это зависит от степени загрязнения воды.
Технический прогресс дает возможность рассчитывать на усовершенствование существующих ныне, а также разработку новых методов очистки воды. Постоянно остается актуальной проблема избавления от находящегося в воде железа. Поэтому развитие новых технологий в этой области остается лишь вопросом времени.
Смотрите также:
www.bwt.ru
Удаление из воды кислорода и углекислого газа
Г. Овчинников
Растворенные в воде кислород и углекислый газ повышают скорость коррозии стали, особенно при повышенных температурах. Поэтому их положено максимально удалять из котловой воды и воды отопительных систем. В данной публикации предлагается обзор направленных на это современных способов водоподготовки
Котловые системы по их назначению принято подразделять на водогрейные и паровые, поэтому для каждого типа существует свой набор требований к очищенной воде, которые также зависят от мощности и температурного режима.
 Разработку официальных требований осуществляют надзорные органы, однако они всегда мягче рекомендаций производителя, устанавливаемых исходя из гарантийных обязательств. Кроме того, в европейском Союзе эти документы проходят всестороннюю экспертизу в органах стандартизации и профильных организациях с точки зрения эффективности и длительной эксплуатации котла. Поэтому целесообразно ориентироваться именно на рекомендации производителя.
Разработку официальных требований осуществляют надзорные органы, однако они всегда мягче рекомендаций производителя, устанавливаемых исходя из гарантийных обязательств. Кроме того, в европейском Союзе эти документы проходят всестороннюю экспертизу в органах стандартизации и профильных организациях с точки зрения эффективности и длительной эксплуатации котла. Поэтому целесообразно ориентироваться именно на рекомендации производителя.
Установка с зернистым редокситом для удаления кислорода из подпиточной воды пеллетных котлов Национального Ботанического сада им. Н.Н. Гришко
Все многообразие водно-химических режимов регламентируется Правилами технической эксплуатации, а также различными руководящими документами, относящимися к отдельным из перечисленных режимам. Только соблюдение правильного водного и химического режимов обеспечит надежную, безаварийную и долговечную работу котельного оборудования, наряду с системами теплоснабжения.
Вред растворенных в котловой воде газов
Также необходима нейтрализация свободной СО2 в оборотных конденсатах нагревательных систем.
Для удаления кислорода из питательной воды котлов можно использовать как физические, так и химические методы. Обычно их комбинируют, сначала — физические, затем химические методы.
Физические методы
К физическим методам относят применение деаэраторов, которые бывают термическими и вакуумными. Для деаэрации воды также разработаны электромагнитный, высокочастотный и ультразвуковой способы, а также пузырьковый азотный.
Наибольшее распространение в паровых и водогрейных котельных получил термический способ. Он основан на процессах, описанных в законе Генри. Согласно с ним, растворимость идеальных газов в воде при постоянной температуре и невысоком давлении прямо пропорциональна парциальному давлению данных газов над водой. Повышение температуры до уровня насыщения при данном давлении снижает до нуля парциальные давления газов над водой, следовательно, и растворимость газов в воде снижается до нуля. Вследствие нарушения равновесия в системе происходит выделение газов из воды (физическая десорбция).
Подбирая такие соотношения температуры и давления, при которых газы становятся практически нерастворимыми, можно почти полностью удалить их из воды.
За последние годы конструкции аппаратов для удаления газов были значительно улучшены. В настоящее время имеется несколько удачных типов деаэраторов, каждый из которых приспособлен для специальной цели. Существуют установки для деаэрации холодной воды без нагревания, дающие 15000 м3 в день и снижающие содержание кислорода до 0,22 мл/дм3. Вода в таком аппарате разбрызгивается по специальным лоткам камеры, находящейся под низким давлением. Газы могут удаляться паровыми эжекторами с холодильниками или вакуумными насосами.
В паровых котельных применяются в основном смешивающие десорберы атмосферного типа низкого избыточного давления. В таком аппарате струйки воды движутся вниз навстречу поступающему из парораспределительной камеры пару, и, соприкасаясь с ним, нагреваются до температуры кипения, в результате чего из воды выделяется растворенный в ней воздух.
В устройстве поддерживается давление 0,12 МПа, а вода нагревается до 104°C, т.е. до температуры кипения при этом давлении. Испарившаяся вода и воздух через штуцер направляются в теплообменник для подогрева воды, поступающей в аппарат. Номинальная производительность таких деаэраторов 25–300 т/ч.
В котельных с водогрейными котлами, где нет пара, используются вакуумные деаэраторы, в которых поддерживается давление около 0,03 МПа при температуре кипения около 69°C. Такое разрежение создается при помощи водоструйного эжектора.
Главным условием удаления газов из горячей воды является поддержание ее в тонкораспыленном состоянии (в течение достаточного времени) при температуре кипения, соответствующей давлению, при котором растворенные газы свободно выделяются в газообразную фазу. При простом типе открытого нагревателя питательной воды деаэратор, при нагреве до 88—93°C и свободном отводе газов в атмосферу, снижает концентрацию кислорода приблизительно до 0,3 мл/дм3.
Устройства для удаления кислорода для систем горячего водоснабжения для больших зданий и комплексов зданий устроены иначе. Воду нагревают под вакуумом так, чтобы температура кипения ее не превышала 60—80°C при помощи рядов змеевиков с греющим паром. Затем воду разбрызгивают вниз по тарелкам. Температура пара, поступающего в нижние змеевики, выше температуры воды, которая вследствие этого испаряется; пар увлекает выделившиеся газы через клапан, охлаждаемый входящей холодной водой. Конденсат из клапана стекает обратно, в тарелочную камеру, в то время, как газы выбрасываются вакуумным насосом или паровым эжектором.
если устройство помещается в подвале здания, то требуется циркуляционный насос для горячей воды, иногда его устанавливают в чердачных технических этажах здания, чтобы подача воды реализовывалась за счет естественной циркуляции. В таких условиях достигается концентрация кислорода 0,04 мл/дм3, что обеспечивает защиту системы от коррозии при температуре ниже 70°С.
В деаэраторах для котловой питательной воды осуществляется прямой контакт воды с паром. Чаще всего применяются аппараты тарелочного типа, работающие под давлением или вакуумом. Десорбер с распылением, работающий под небольшим давлением, широко применяется в котельных установках. В деаэраторе тарелочного типа холодная питательная вода проходит через холодильник, затем поступает в камеру, нагреваемую паром, где разбрызгивается на металлические тарелки. После этого вода стекает в резервуар для хранения. Пар наполняет все пространство, причем направление его движения таково, что он нагревает воду и удаляет выделяющиеся газы. Таким образом, можно достигнуть практически полного отсутствия кислорода в воде.
В более современной модели деаэратора происходит распыление воды в атмосферу пара при давлении приблизительно 0,1 кг/см2. Этот тип десорбера разработан для судовых котлов. Устройство состоит из холодильника, секции с паровым обогревом, деаэрационной секции, окружающей впуск пара, и секции для хранения деаэрированной воды, расположенной внизу аппарата. Холодная питательная вода проходит через холодильник, затем через распыляющие форсунки, поступает в камеру, обогреваемую паром, и снова через форсунки в деаэрационную камеру, а затем в водосборник. Пар входит в деаэрационную камеру под давлением 0,7 кг/см2 и подымается в холодильник, где выпускаются удаляемые газы, а теплота пара передается воде, поступающей в аппарат. Большая часть растворенного кислорода удаляется из воды при первоначальном ее нагревании; последние 5% кислорода удаляются значительно труднее. Для этого служит деаэрационная камера, которая обеспечивает практически полное удаление кислорода из воды.
Наиболее мощные деаэраторы удаляют также всю свободную двуокись углерода и частично — полусвязанную углекислоту и другие газы. При этом, вследствие отсутствия двуокиси углерода, рН воды увеличивается.
Существует безреагентная технология глубокого удаления кислорода для паровых и водогрейных систем, с использованием гидрофобных мембран в контакторах, что позволяет достигать глубокой степени очистки воды – до 1 мкг/дм3.
Применение десорбционных методов позволяет удалять газ до известного предела, недостаточного в ряде случаев по условиям использования воды. Кроме того, не всегда имеется возможность и необходимость включения в схемы сложных аппаратов для газоудаления. Поэтому на многих теплоэлектростанциях для обработки питательной и добавочной воды применяются химические методы связывания O2 и CO2 в вещества, являющимися безопасными в коррозионном отношении.
Химические методы
В основе химических методов удаления из воды растворенных газов лежит их химическое связывание, достигаемое введением реагентов или фильтрованием через специальные загрузки.
Для извлечения из воды кислорода применяют ее фильтрование через легко окисляющиеся вещества, например, стальные стружки, другие регенерируемые загрузки.
Степень удаления свободного кислорода для предотвращения коррозии котлов и сетей, зависит от температуры теплоносителя, объема воды.
Обычно при 70°, как это имеет место во многих системах ГВС, не требуется уменьшение содержания кислорода ниже 0,07 мл/дм3. Для паровых котлов, работающих под давлением ниже 17,5 кг/см2 (без экономайзеров) желательный предел не должен превышать примерно 0,02 мл/дм3. Для котлов высокого давления (или при применении экономайзеров) требуется практически полное отсутствие кислорода, т. е. ниже 0,0035 мл/дм3.
Содержание O2 в системах холодной воды при одноступенчатой аэрации достигает значения не более 0,2 мл/дм3, а при условии содержания кислорода менее 0,07 мл/дм3, применяется дополнительная обработка воды, выходящей из деаэратора, дозированием химических препаратов.
Существует много реагентов и их композиций под разными коммерческими названиями, которые могут быть использованы для нейтрализации кислорода. У каждого реагента есть свои положительные и отрицательные свойства и качества. Они будут рассмотрены ниже.
Самым распространенным реагентом для химического удаления кислорода из воды служит сульфит натрия Na2SO3 под разными фирменными названиями. Как в чистом виде, так и в виде каталитически активной формы. В качестве катализаторов используют оченьнебольшие количества меди или кобальта.
Рекомендуемые концентрации сульфита натрия у разных авторов значительно отличаются. Для удаления 1 кг кислорода требуется около 8 кг сульфита натрия, однако есть много рекомендаций по дозированию избыточного количества этого катализатора – от 2 до 40 мг/дм3 для конкретных котлов и режимов работы.
Обработка воды с помощью Na2SO3 основана на реакции окисления сульфита растворенным в воде кислородом:
2Na2SO3 + O2 = 2Na2SO4.
В этой реакции в качестве восстановителя выступает четырехвалентная сера S4+, которая отдает электроны кислороду, окисляясь до S6+.
Важным показателем процесса связывания кислорода является скорость реакции между сульфитом натрия и кислородом. Она зависит от температуры обрабатываемой воды и, в соответствии с законом действия масс, — от количества вводимого реагента.
Так, при температуре воды 40°C и дозировке стехиометрического количества сульфита натрия процесс завершается за 6—7 минут, при температуре 80°C время реакции составляет немногим более 1 минуты. При 70% избытке реагента, в соответствии с законом действия масс, реакция протекает до конца в течение 2 минут при любой температуре.
При температуре свыше 275°C (давление насыщения 6 МПа) сульфит натрия может разлагаться с образованием SO2 или h3S, что заметно увеличивает скорость коррозии оборудования пароконденсатного тракта.
Поэтому данный реагент может быть использован только для обескислороживания воды котлов среднего давления (3–6 МПа), испарителей и для подпиточной воды тепловой сети.
Раствор сульфита натрия концентрацией 3–6% готовят в баке, защищенном от контакта с атмосферой, и затем, с помощью дозатора, вводят в обрабатываемую воду с некоторым избытком против стехиометрического количества.
Однако передозировка реагента во много раз повышает электропроводность котловой воды (содержание солей), а также шламообразование, возможны проблемы в связи с образованием пены в котловой воде.
Сульфитирование просто в осуществлении, не требует громоздкой и дорогой аппаратуры. Недостатком данного метода является то, что оно увеличивает сухой остаток в количестве 10–12 мг/дм3 на 1 мг/дм3 растворенного кислорода.
Разработана и применяется оригинальная эффективная технология по удалению O2 из воды с применением зернистого фильтрующего материала, изготовленного на основе синтетических ионитов макропористой структуры, в которую встраиваются активные центры металлов, в частности, двухвалентного железа.
В процессе фильтрации воды через слой загрузочного материала окисление растворенным кислородом переводит закисные формы железа (FeO) в двойной оксид железа (FeO•Fe2O3nh3O) или в полутораокиси (Fe2O3•nh3O).
Сущность технологического процесса заключается в применении сорбента, имеющего достаточно высокую емкость поглощения по кислороду (т.е. представляющего собой редоксит в восстановленной форме). В качестве такого сорбента использован ионитный комплекс с переходным металлом, введенным в фазу ионита.
При этом процесс химического поглощения кислорода можно представить в виде следующего уравнения:
4RMe(ОН)n + О2 + 2h3O →4RMe(OH)(n+1),
где R – нерастворимый в воде сложный радикал ионита;Ме – переходной металл.
По мере фильтрации воды через слой редоксита все большая его часть будет переходить в окисленную форму и, наконец, способность к дальнейшему поглощению кислорода будет полностью исчерпана. По истечению рабочего цикла Redox-фильтра истощенный сорбент подвергается регенерации.
Регенерация представляет собой процесс восстановления поглотительной способности редоксита путем пропуска через слой, например, тиосульфата натрия:
RMe(ОН)n + 2h3O →4RMe(OH)(n-1),
где R – нерастворимый в воде сложный радикал ионита;Ме – переходной металл.
Перед пропуском регенерационного раствора редоксит необходимо взрыхлять обратным током воды. После его отмывают от избытка реагента и продуктов регенерации.
Для барабанных котлов высоких и сверхвысоких давлений применяется гидразин в форме гидразин-гидрата или гидразин-сульфата, которые энергично взаимодействуют с кислородом, окисляясь в итоге до воды и азота, т.е. не повышая солесодержания воды:
N2h5·h3O + O2 = 3h3O + N2.
Гидразин-гидрат можно успешно применять для обработки питательной воды как барабанных, так и прямоточных котлов (он не повышает сухого остатка воды), в то время как гидразин-сульфат — только для обработки питательной воды барабанных котлов (он несколько увеличивает сухой остаток).
Скорость реакции зависит от температуры, pH среды, избытка гидразина, в соответствии с законом действия масс, а также присутствия катализаторов. При температуре менее 30°C гидразин практически не взаимодействует с O2, но при 105°C, pH = 9–9,5 и избытке гидразина около 0,02 мг/дм3 время практически полного связывания кислорода составляет несколько секунд.
Гидразин вводится в воду в виде 0,1–0,5% раствора с избытком против стехиометрического количества с учетом того, что часть его расходуется на восстановление высших оксидов железа и меди из отложений на трубах.
Гидразин-сульфат может применяться при любых давлениях, однако наиболее целесообразно использовать его только при давлении 70 кгс/см2 и выше, а при низком давлении лучше применять сульфит натрия вследствие его меньшей стоимости.
Расчет дозы гидразина g (мкг/кг) в пересчете на Nh5рекомендуется производить по формуле:
g=С1+0,35С2+0,15С3+0,25С4+40,
где С1 — концентрация кислорода в питательной воде до ввода гидразина, мкг/кг;С2 – концентрация нитритов в питательной воде до ввода гидразина, мкг/кг;С3 – концентрация железа в питательной воде, мкг/кг;С4 – концентрация меди в питательной воде, кг/кг.
Концентрация гидразина в рабочем растворе С (мг/кг) рассчитывается по формуле:
С = D/DH,
где D – расход питательной воды, т/ч;DН – средняя (регулируемого диапазона) подача насоса-дозатора, л/ч.
При приготовлении рабочего раствора гидразин-сульфата, последний должен быть нейтрализован едким натром. его количество, необходимое для нейтрализации, y (кг) рассчитывается по формуле:
у=0,62у1+0,04ЩVб,
где у1 – количество загружаемого гидразинсульфата, кг;Щ – щелочность по фенолфталеину воды, используемой для приготовления рабочего раствора, мг-экв/кг;Vб – объем бака, м3.
В котловой воде и в пароперегревателях избыток гидразина разлагается с образованием аммиака:
3N2h5 = 4Nh4 + N2.
При организации гидразинной обработки воды следует учитывать, что гидразин является высокотоксичным и канцерогенным веществом, при концентрации выше 40% он горюч, поэтому должны предусматриваться специальные строгие меры безопасности.
Для связывания кислорода в котловой воде могут применяться и другие органические и неорганические соединения. Например гидрохинон (парадиоксибензол), пирогаллол (несимм-триоксибензол), изоаскорбиновая кислота, карбогидразин, N, N-диэтилгидроксиламин (ДЭГА). Их применение регламентируется рекомендациями производителя конкретного оборудования.
Все вышеперечисленные химические соединения могут входить в рецептуру многих комплексных фирменных составов для обработки котловой воды и внутрикотловых поверхностей.
Углекислота, поступающая в пароводяной цикл через различные воздушные неплотности оборудования, а также и за счет разложения карбонатов солей (в добавочной воде), приводит к понижению рН воды. Это, в свою очередь, усиливает процессы коррозии за счет взаимодействия водородных ионов с металлом, а также за счет снижения защитных свойств окисной пленки на поверхности металла. Вследствие этого углекислота всегда является фактором усиления коррозии.
Для предотвращения углекислотной коррозии оборудования конденсатно-питательного тракта ТЭС с барабанными котлами применяется способ связывания свободной углекислоты путем ввода в конденсат турбин или питательную воду щелочного реагента – водного раствора аммиака. Основной задачей такой обработки является повышение pH воды и конденсата на участках пароводяного тракта, что надежно обеспечивает защиту оборудования от коррозии с водородной деполяризацией.
Дозировка аммиака определяется его количеством, необходимым для связывания диоксида углерода в гидрокарбонат аммония. Небольшой избыток Nh4 сверх этого количества образует уже карбонат аммония и повышает pH воды до значений выше 8,5:
Nh4 + h3O + CO2 = Nh5HCO3,Nh5HCO3 + Nh4 = (Nh5)2CO3.
Из приведенных уравнений следует, что для связывания 1 мг/дм3 CO2 достаточно 0,26 мг/дм3 аммиака.
Аммиак обычно вводится в обрабатываемую воду в виде 1–5% раствора Nh5OH с помощью насосов-дозаторов, автоматизированных по расходу воды. При концентрации свободной углекислоты в воде или паре свыше 8 мг/дм3 применение аммиака обычно недопустимо, так как может протекать коррозия медных сплавов (латуни), применяющихся для изготовления оборудования конденсатно-питательного тракта.
Разработан и применяется комбинированный гидразино-аммиачный режим,который характеризуется вводом в теплоноситель (в основном в питательную воду) аммиака в целях повышения рН воды и нейтрализации воздействия углекислоты, а также вводом гидразина с целью снижения содержания остаточного кислорода после деаэраторов питательной воды. Благодаря воздействию высокого значения рН, замедляются коррозионные процессы стали и медных сплавов. Однако аммиак, помимо способности к повышению рН аминируемой воды, обладает также способностью специфического коррозионного воздействия на медные сплавы. Поэтому доза аммиака при введении гидразино-аммиачного режима ограничивается поддержанием в питательной воде содержания аммиака на уровне, не превышающем 1 мг/дм3.
Больше важных статей и новостей в Telegram-канале AW-Therm. Подписывайтесь!
Вам также может понравиться
aw-therm.com.ua
Удаление кислорода из воды - ООО НПП «НЦВТ»
Кислород в воде необходим, он – источник питания для бактерий, микроорганизмов. Но этот элемент – окислитель, повышенное его содержание в воде способствует преждевременному выходу из строя оборудования, трубопроводов, являясь катализатором коррозии. В воде кислород находится в растворенном состоянии. Вода из подземных источников содержит его в малых концентрациях, а из поверхностных – в больших.
Каким должно быть содержание кислорода в воде, чтобы трубы и другие металлические элементы конструкции не повреждались, зависит в основном от рабочей температуры и в некоторой степени от количества жидкости, протекающей через систему.
В сооружениях, по которым течет холодная вода, допустимая концентрация кислорода в воде не должна быть выше 0,2 мл/л. Если требуется достичь параметра меньшего, чем это возможно при обычной деаэрации, необходима дополнительная обработка выходящей оттуда воды. Для этого могут использоваться вспомогательные химические реагенты или же еще одна процедура деаэрации.
В основном системы снабжения горячей водой транспортируют ее при температуре 70°, с целью сбережения элементов от коррозии достаточно будет снизить концентрацию кислорода до 0,07 мл/л.
При эксплуатации паровых систем отопления, давление в которых не превышает 17,5 кг/см2, предельное содержание кислорода составляет 0,02 мл/л. Если используется оборудование с высоким давлением или же установлены экономайзеры, желательно добиться практически полного отсутствия кислорода в воде, его концентрацию надо снизить до 0,0035 мл/л и ниже.
Способы снижения концентрации в воде растворенного кислорода
Термический метод – заключается в том, что нагретая до температуры 70°С вода соприкасается с перфорированным железным листом, имеющим большую площадь поверхности. Длится весь процесс не менее получаса, во время взаимодействия железа с водой кислород практически полностью расходуется на коррозию. Также может использоваться железный лом. Для совершения такой процедуры требуется сложное громоздкое оборудование, оснащенное песочными фильтрами. Оно сложное в уходе, требует больших затрат во время эксплуатации. Термический метод практически вытеснен физическим удалением излишков кислорода – деаэрацией.
Использование сернистонатриевой соли может быть экономически оправданным только в том случае, если перед этим проводилась предварительная деаэрация, во время которой была удалена большая часть свободного кислорода. При удалении 1 кг растворенного в воде кислорода затраты сернистонатриевой соли составят больше 8 кг. С целью полного удаления кислорода в отопительных системах потребуется 30 мг избыточной сернистонатриевой соли на каждый литр. Значительно реже применяется для деаэрации серножелезистая соль. Она должна быть нейтрализована едким натром.
Достаточно большой эффективностью обладает химически-коррекционный способ. В основную массу воды добавляется реагент, вступающий в реакцию с растворенным кислородом. Лучшего результата можно достичь в сочетании с термическим воздействием на воду, то есть, ее необходимо нагреть до 70° и выше. Как правило, в качестве реагента используется водный раствор сульфита натрия, также может применяться катализированный бисульфит натрия.
При вступлении реагента в реакцию с растворенным кислородом возникает избыток сульфит-ионов, поддерживаемый на уровне 2-3 мг/л. Также могут создаваться условия для образования избытка SO32-, который будет постоянно находиться на уровне 2-3 мг/л.
Назад в разделncwt.ru
Способ удаления из воды кислорода
Изобретение может быть использовано на химводоочистках котельных производственных и иных предприятий, получающих горячую сетевую воду, в производстве натрийкатионированной воды для питания паровых котлов. Для осуществления способа ведут фильтрацию воды через высокоосновной анионит AM гелевой структуры в SO3-форме. Время контакта воды с ионитом не менее 7,5 мин. Регенерацию отработанного анионита производят раствором сульфита натрия с концентрацией не выше 8%. Способ обеспечивает повышение эффективности удаления из воды кислорода. 1 з. п. ф-лы, 2 табл.
Изобретение предназначено для удаления кислорода из воды на химводоочистках (ХВО) котельных производственных и иных предприятий, получающих горячую сетевую воду. Особенно перспективно применение изобретения в производстве Na-катиониро-ванной воды для питания (или подпитки) паровых котлов.
Наиболее универсальным методом удаления из воды растворенного кислорода для обработки большинства водопроводных вод является вакуумная деаэрация /Лосев В. Л. Электрохимическое обескислороживание воды в системах горячего водоснабжения. Водоснабжение и санитарная техника, 1965, N3, с. 18-23/. К недостаткам метода относятся значительные габариты аппаратов, что вынуждает увеличивать помещение теплового пункта по площади и высоте и высокие стоимостные показатели сооружения установки. Известен способ удаления растворенного в воде кислорода путем применения специальных электронообменных смол с введенными в них катионами железа или меди. Выпускаемая промышленностью электронообменная смола ЭИ-12 имеет поглотительную способность по кислороду 45 кг O2/м3 /Справочник проектировщика. Водоснабжение населенных мест и промышленных предприятий. -М.: Стройиздат, 1977, c.230/. Недостатком данного способа является низкая поглотительная способность материала, приводящая к частому осуществлению операции регенерации ЭИ-12, и низкая химическая устойчивость электронообменного ионита относительно востановителей. Так, регенерация отработанного ЭИ-12 осуществляется растворами сульфита или тиосульфата натрия концентрацией не выше 1-2%. Применение для регенерации таких разбавленных растворов приводит к увеличению продолжительности операции регенерации и объемов сбрасываемых промывных вод. Задачей данного изобретения является повышение эффективности удаления из воды кислорода путем пропускания исходной воды через высокоосновной анионит AM гелевой структуры, получающийся последовательно реакциями хлорметилирования и аминирования триметиламином гранульного сополимера стирола с 4-8% ДВБ (Ласкорин Б.Н., Иоанисиани П.Г., Никульская Г.Н. Синтез новых ионитов. - В кн. :Ионообменные сорбенты в промышленности. Изд-во АН СССР, 1963, с.21-31), находящийся в рабочей сульфитной форме. Причем время контактирования воды с анионитом составляет не менее 7,5 минут, так как при меньшем времени контактирования происходит резкое увеличение содержания кислорода в фильтрате даже при относительно небольшом количестве пропущенной воды, обусловленное, вероятно, уменьшением эффективности диффузии кислорода к поверхности анионита из-за сокращения времени контакта последнего с водой. Регенерация отработанного анионита осуществляется раствором сульфита натрия концентрацией не выше 8%. При концентрации регенерирующего раствора сульфита натрия более 8% происходит заметное снижение емкости анионита по сульфит-иону (табл.2), изменение цвета анионита от желтого до черного, обусловленное разрушением последнего при контакте с высококонцентрированным раствором восстановителя. Пример. Через высокоосновной анионит гелевой структуры AM, находящейся в сульфитной форме, пропускалась водопроводная вода (СO2 - 9,2 мг/дм3 при 21,2oС) со скоростью 75 см3/ч. Время контакта 7,5 мин. Объем анионита в колонке диаметром 10 мм составлял 10 см3. Регенерация отработанного анионита осуществлялась (после появления фильтрата с содержанием растворенного кислорода 1,0 мг/дм3) раствором 8% сульфита натрия. В табл.1 и 2 представлены результаты экспериментов. При фильтровании исходной воды через слой анионита AM, находящейся в сульфитной форме, происходит окисление растворенным в воде кислородом - сульфит-иона анионита до SО4. Эффективность массообменного процесса обеспечивает низкое содержание кислорода в обработанной воде (не более 1,0 мг/дм3) в течение значительной продолжительности фильтроцикла. Регенерация анионита осуществляется по достижении им значения поглотительной способности по кислороду не более 180 мг О2/дм3. При больших значениях поглотительной способности анионита возможно ухудшение качества фильтрата по кислороду (более 1,0 мг О2/дм3). Высокая химическая устойчивость анионита в востановительной среде позволяет осуществлять регенерацию анионита AM раствором сульфита натрия концентрацией 8%, что в четыре-восемь раз превосходит концентрацию раствора для случая регенерации материала прототипа (ЭИ-12). При больших концентрациях раствора Na2SO3 происходит заметное снижение содержания сульфит-иона в анионите (емкости), а следовательно, и поглотительной способности анионита по кислороду.Формула изобретения
1. Способ удаления из воды кислорода, заключающийся в фильтрации воды, содержащей растворенный кислород, через ионит с последующей регенерацией, отличающийся тем, что фильтрацию осуществляют через высокоосновный анионит AM гелевой структуры в SО3-форме, а регенерацию отработанного анионита производят раствором сульфита натрия с концентрацией не выше 8%.2. Способ по п.1, отличающийся тем, что время контакта исходной воды с ионитом составляет не менее 7,5 мин.РИСУНКИ
Рисунок 1Похожие патенты:

Изобретение относится к установкам непрерывного действия для опреснения морских, соленых вод и электропроводных растворов и может быть использовано для переработки загрязненных сточных вод промышленных предприятий, в том числе нефтепродуктами, а также для получения подпиточной воды котлов тепловых и электрических станций

Изобретение относится к способам выделения ионов тяжелых металлов сорбцией на целлюлозосодержащих сорбентах из растворов различной природы, образующихся после проведения разнообразных технологических процессов, и может быть использовано для совершенствования мембранных и сорбционных технологий

Изобретение относится к способу удаления азотсодержащих гетероциклических или ароматических соединений, содержащих, по меньшей мере, одну нитрогруппу

Изобретение относится к электрохимическим способам очистки сточных вод, в частности сточных вод текстильной промышленности, содержащих красители

Изобретение относится к очистке воды и может быть использовано при обессоливании природных и сточных вод

Изобретение относится к санитарно-гигиенической обработке воды и других жидкостей и может быть использовано как самостоятельно, так и в составе систем обеззараживания жидких продуктов

Изобретение относится к обработке добываемой воды из установки добычи сырой нефти тепловым методом для достижения уровня извлечения и рециркуляции воды от более 80 до 100% при достижении нулевого сброса

Изобретение относится к аналитической химии радиоактивных элементов, а именно к способам концентрирования радионуклидов с одновременным выделением их

Изобретение относится к области очистки сточных вод и может быть использовано для очистки хромсодержащих сточных вод при организации оборотного водоснабжения, для очистки промывных вод гальванических производств от тяжелых металлов и ряда органических веществ, очистки маслоокалиносодержащих сточных вод, мышьяксодержащих растворов, для очистки стоков предприятий горной, металлургической, химической и других отраслей промышленности [1]

Изобретение относится к водоснабжению и может быть использовано при доочистке и обеззараживании питьевой воды

Изобретение относится к установкам непрерывного действия для опреснения морских, соленых вод и электропроводных растворов и может быть использовано для переработки загрязненных сточных вод промышленных предприятий, в том числе нефтепродуктами, а также для получения подпиточной воды котлов тепловых и электрических станций

Изобретение относится к способам выделения ионов тяжелых металлов сорбцией на целлюлозосодержащих сорбентах из растворов различной природы, образующихся после проведения разнообразных технологических процессов, и может быть использовано для совершенствования мембранных и сорбционных технологий

Изобретение относится к способу удаления азотсодержащих гетероциклических или ароматических соединений, содержащих, по меньшей мере, одну нитрогруппу

Изобретение относится к электрохимическим способам очистки сточных вод, в частности сточных вод текстильной промышленности, содержащих красители

Изобретение относится к очистке воды и может быть использовано при обессоливании природных и сточных вод

Изобретение относится к санитарно-гигиенической обработке воды и других жидкостей и может быть использовано как самостоятельно, так и в составе систем обеззараживания жидких продуктов

Изобретение относится к обработке добываемой воды из установки добычи сырой нефти тепловым методом для достижения уровня извлечения и рециркуляции воды от более 80 до 100% при достижении нулевого сброса

Изобретение относится к аналитической химии радиоактивных элементов, а именно к способам концентрирования радионуклидов с одновременным выделением их

Изобретение относится к области очистки сточных вод и может быть использовано для очистки хромсодержащих сточных вод при организации оборотного водоснабжения, для очистки промывных вод гальванических производств от тяжелых металлов и ряда органических веществ, очистки маслоокалиносодержащих сточных вод, мышьяксодержащих растворов, для очистки стоков предприятий горной, металлургической, химической и других отраслей промышленности [1]

Изобретение относится к водоснабжению и может быть использовано при доочистке и обеззараживании питьевой воды

Изобретение относится к аппаратному оформлению процесса в гетерогенной системе жидкость - твердое тело, например сорбция, выщелачивание, растворение
Способ удаления из воды кислорода
www.findpatent.ru
Аэрация воды из скважины: принципы обезжелезивания
В современной водоочистке применяются разные способы удаления примесей из воды. Соли железа вредны и для здоровья, и для внутренних деталей, узлов очистных систем. Избавиться от них можно путем обезжелезивания. Самый эффективный вариант – аэрация воды. Он предполагает искусственное создание интенсивного воздухообмена, в результате которого происходит активное насыщение воды кислородом, окисление железа, выпадение растворенного в воде железа в осадок, очистка и нормализация состава воды.
Очистка воды с помощью метода аэрации: суть метода
Аэрация производится для преобразования растворенных соединений марганца и железа, которые есть в воде, в окислы. В данном виде они потом выпадают в осадок в виде хлопьев, которые затем задерживаются фильтрами очистных систем. Затем происходит окисление с последующей отдувкой летучих соединений. Эти соединения являются токсичными и имеют неприятный запах. Воду с высокой концентрацией солей железа в бытовых целях использовать нельзя, поскольку данные вещества будут оседать на рабочих деталях и узлах сантехники, негативно влияя на их внешний вид и функциональность. Вредны соли железа и для здоровья – постоянное употребление в пищу воды, с избытком железа, негативно сказывается на самочувствии человека, нарушает нормальную работу его органов и систем.
Необходимость обезжелезивания воды. Виды очистки аэрацией

Системы аэрации широко используются для очистки воды от железа в производственных и бытовых целях. Жидкость, богатая соединениями железа, органическими загрязнителями и летучими веществами, требует обязательного проведения предварительной очистки, которая заключается в окислении посторонних включений. Способы окисления существуют разные, но одним из наиболее популярных является именно аэрация. Почему? Потому что она производится без использования химических реагентов и является максимально безопасной. Вместо опасной химии используется кислород.
Основные цели использования аэрации воды из скважин:
- удаление солей железа;
- устранение посторонних ароматов;
- биологическая обработка;
- повышение концентрации кислорода.
Преимущества обезжелезивания воды аэрацией
Системы аэрации имеют следующие преимущества:
- Компактные размеры – благодаря этому, устанавливать комплексы можно на небольших участках и внутри жилых домов.
- Доступная стоимость – цена очистки получается более чем доступной. Точно сказать, во сколько вам обойдется эксплуатация такой системы, можно будет с учетом ее мощности, производительности и выбранного типа оборудования.
- Автоматическая работа – аэрационные установки функционируют полностью автономно.
- Неприхотливость в обслуживании – модули в дополнительном обслуживании не нуждаются, поэтому временные и финансовые затраты на обеспечение нормальной работоспособности техники получаются минимальными.
Способы аэрации воды

Выбор способа аэрации зависит от напора воды и других факторов. Основные варианты:
- Электрохимический – самая современная методика. Принцип работы оборудования основывается на применении электрохимических реакций, превращающих химическую и электрическую форму энергии в электрохимическую. Данная методика обеспечивает эффективную очистку воды с повышенным содержанием солей железа. Преимущества электрохимических аэрационных комплексов – невысокий уровень шума, экономичность в эксплуатации, небольшие габариты, простое обслуживание (в зимнее время года тоже).
- Напорный – данный способ применяется при сильном магистральном напоре и сравнительно невысоком содержании солей железа (оно не должно превышать 15 мг/л). Когда жидкость поступает под напором в колонну, срабатывает датчик потока, компрессор включается в работу, и воздух начинает закачиваться внутрь устройства. Кислород, который содержится в воздухе, обогащает воду, после чего производится ее фильтрация.
- Безнапорный – методика подходит для очистки воды при низком давлении и небольшом магистральном напоре, содержании железа до 15 мг на литр. В безнапорных системах аэрации воды содержится бак, в который и поступает разбрызгиваемая форсунками жидкость. Компрессор также дополнительно обогащает ее кислородом, но в фильтр жидкость попадает благодаря работе насоса.
- Упрощенный – данный способ аэрации применяется при невысоком содержании и железа, и сероводорода, нейтральной кислотности жидкости. Он предполагает слив воды в карман либо канал магистрали. Окислительного бака в составе конструкции нет, что существенно снижает стоимость системы, но ограничивает ее функционал и сферы применения.
Как провести аэрацию и очистку воды
Во всех рассмотренных выше установках применяется одна и та же методика аэрации. Процесс очистки состоит из следующих этапов:
- Вода насыщается кислородом и окисляется до состояниях трех или двухвалентного железа. Примеси оседают в виде осадка и остаются на фильтре.
- Осуществляется отдувание растворенных газов, включая сероводород.
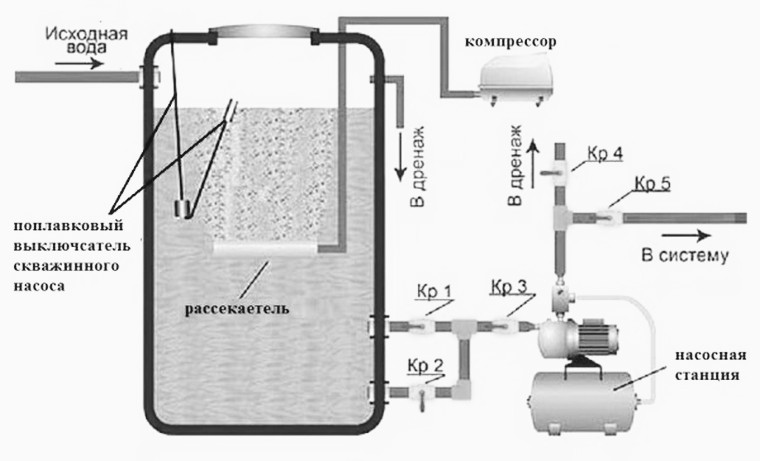
И напорная, и безнапорная методики аэрации позволяют получать чистую питьевую воду, которую можно употреблять для питья и приготовления пищи. При этом жидкость не будет содержать химических реагентов.
Процесс обезжелезивания воды своими руками
В домашних условиях проводить очистку от растворенного железа тоже можно – для этого используются специальные вещества. Они имеют пористую структуру, весят меньше и быстро удаляют различные соединения, включая соли железа. Учтите только, что такие вещества плохо взаимодействуют с хлором – применять и их, и хлор для обеззараживания воды одновременно нельзя. Самые популярные средства для аэрации в домашних условиях – это Birm, «Магнофилт», Greensand, но есть и другие составы. Они имеют схожие принципы действия, но могут отличаться в плане эффективности.
Чтобы создать домашнюю аэрационную систему, возьмите:
- циркулярный насос;
- фильтрующую установку;
- фильтр оптимальной производительности.
Каким должен быть фильтр? Выбирайте устройство, которое очищает от 250 л жидкости в день. Продумайте нюансы обустройства накопительного воздушного резервуара. Накопительный очиститель использовать можно, но не для металлических деталей (если в водопроводе есть железные муфты, фитинги, сгоны, от применения накопительной системы очистки следует отказаться).
Основа домашней системы обезжелезивания воды – резервуар, объем которого составляет 100 литров и более. При включении компрессора начинает осуществляться подача жидкости через распылительную установку (в последствии распыление воды будет происходить уже внутри емкости). Концентрацию кислорода в баке контролирует специальный элемент, а уровень воды в системе – выходные трубки (их две). На трубки нужно натянуть силиконовый материал, а на той трубке, которая используется для вывода воды из емкости, устанавливается компрессор и обратный клапан.
Компактный аэратор для воды. Преимущества и недостатки насадки на кран
Ручной компрессор или воздушный аэратор, устанавливаемый на кран водозабора, уменьшает поток воды. В процессе подачи жидкость смешивается с молекулами воздуха и очищается от частичек песка, солей металлов. Как понять, правильно работает установка или нет? Оценить правильность работы приспособления не так уже и сложно. Первое, на что следует ориентироваться – это на молочный оттенок струи воды на выходе аэратора. Если цвет другой, значит, что-то не так. Кроме того, жидкость не должна распыляться – она как бы обтекает насадку.
Материалы для изготовления компактных аэраторов используются разные, но лучше всего использовать нержавеющие или с никелированной поверхностью сплавы. Пластик – вариант рабочий, но недолговечный, кроме того, пластиковые насадки плохо выдерживают сильные потоки воды.
Преимущества насадок:
- дешевизна;
- невысокая шумность;
- неприхотливость в обслуживании.
Минус у правильно установленных, качественных систем только один – это недолговечность. Не забывайте своевременно очищать насадку – для этого аэратор снимается с крана, резиновая прокладка очищается или заменяется, достается цилиндр с сетками. Очистить нужно будет все сборные элементы системы.
Аэрация – простой, эффективный, безопасный и сравнительно недорогой способ водоочистки. Его используют многие владельцы загородных участков, которые хотят быть уверены в высоком качестве воды, используемой в пищевых целях. Способы аэрации применяются разные, выбор оптимального следует осуществлять с учетом количественного содержания в воде солей металлов и других примесей. Вы можете использовать как крупные очистные системы аэрации, так и насадки на кран.
global-aqua.ru
Очистка воды от марганца: особенности и методы
Текущие санитарные нормы ограничивают предельно допустимое содержание марганца в хозяйственной и питьевой воде – допустимая норма составляет 0,1 мг/л. В некоторых европейских странах требования еще жестче – до 0,05 мг/л. Если содержание элемента выше, страдают органолептические свойства воды, появляется неприятный привкус, на сантехнике образуются характерные пятна, а на трубах собирается осадок (он имеет вид черной пленки). В подземных водах элемент содержится в виде растворимых солей Mn2+. Чтобы очистить воду от марганца, его сначала нужно перевести окислением в нерастворимое состояние, после чего начнутся процессы гидролизации с образованием нерастворимых гидроксидов Mn(OH)3, Mn(OH)4. При осаждении на загрузке фильтра начинает проявлять каталитические свойства, ускоряя окисление двухвалентного марганца кислородом. Для эффективного окисления элемента кислородом нужно, чтобы значение рН воды, которая проходит очистку, находилось в районе 9.5-10.0. Перманганат калия, гипохлорит натрия или хлор, озон позволяют вести процессы демаганации при меньших показателях рН – например, 8.0-8.5. Для окисления 1 мг марганца, растворенного в воде, требуется около 0.291 мг кислорода.
Очистка воды от железа и марганца: обезжелезивание и деманганация (удаление марганца). Нужно ли очищать воду из скважины
Железо и марганец – самые распространенные загрязнители водных источников. Вода просачивается через грунтовые минеральные отложения и насыщается катионами данных металлов. Если норма железа превышается, то и содержание марганца часто оказывается критическим. Для исправления ситуации проводится деманганация (процесс удаления марганца из воды).
Марганец, как и железо, может пребывать в двух состояниях – растворенном и окисленном. В подземных источниках кислорода нет, поэтому марганец содержится в них в растворенном виде. Для удаления его из воды в данном случае применяются те же методики, что при обезжелезивании. То есть сначала нужно будет окислить марганец, а затем уже убрать взвеси из воды.
Важность очистки воды от марганца
Избыток марганца придает воде характерный желтый оттенок и вяжущий привкус. От такой воды на трубах и сантехнике появляются темные пятна и черные наросты. Но главное даже не это, а то, что постоянное употребление в пищу тяжелых металлов чревато очень неприятными последствиями (они склонны накапливаться). Негативно влияет избыток марганца на работу ЦНС, состояние сердечно-сосудистой системы и скелета. Во время беременности данный элемент особенно опасен, поскольку он сказывается на развитии ребенка.
Современные способы (методы) и процесс глубокой очистки воды из скважины от марганца. Оборудование и материалы для фильтрации
Важнейшее условие качественной очистки водных масс от марганца – требуемый уровень водородного значения рН, поскольку из-за химического состава окисление данного элемента (в отличие от обычного железа) происходит сложнее. При показателе от pH 7.5 ионы марганца принимают нерастворенную форму, а если он ниже 7.0, эффективное удаление элемента становится просто невозможным. В данном случае в целях повышения водородного показателя могут использоваться фильтры корректоры pH с кальцитом – зернистыми мраморными фракциями.
Для дальнейшей очистки потребуется окислитель, поскольку содержащегося в воде элемента обычно оказывается недостаточно. Решить проблему помогают эжекторы-аэраторы.
Очистка воды от марганца с применением обезжелезивателя
В грунтовых водах, в которых кислорода нет вообще, марганец присутствует в двухвалентной растворенной форме. Чтобы удалить его из воды, сначала нужно будет произвести окислительные реакции, а потом фильтрацию. Хорошие результаты показывают фильтры-обезжелезиватели.
Очистка воды от марганца с применением фильтра комплексной очистки
Фильтры комплексной очистки стоят дороже остальных решений, зато эффективно удаляют марганец при любых заданных значениях pH. Насыщать воду кислородом при этом не требуется. Многокомпонентная фильтрующая среда комплексных установок также гарантирует эффективную очистки воды от железа, солей жесткости, органики и прочих примесей, которые в ней растворены. Данный вид водоочистки очень эффективен в удалении марганца из колодезной и скважинной воды. Один такой фильтр заменяет сразу несколько устройств разного назначения.
Очистка воды от марганца с применением накопительных баков
Также удаление марганца из колодезной воды может производиться с применением накопительных баков. Сначала в целях лучшего окисления выполняется корректировка водородного показателя кальцитом (его засыпают на дно колодца либо в накопительный газ). Окислительные процессы запускает аэрационное устройство – эжектор. После прохождения эжектора насыщенная воздухом вода поступает в накопительную емкость, где продолжаются окислительные реакции. Затем вода начинает подаваться насосной станцией на фильтр промывной титановой мембраны. Частики марганца от 0.1 микрон, которые не смогли раствориться, удерживаются поверхность мембраны.
Принципы работы фильтрационной системы и удаление марганца из воды
На первой стадии очистки из воды вакуумом убирают свободную углекислоту, в результате чего рН повышается до 8.0-8.5. Упрощает выполнение работ вакуумно-эжекционный аппарат, в эжекционной части которого происходит диспергирование воды с последующим насыщением кислородом воздуха. Затем вода подается на фильтрацию через зернистую загрузку (это может быть кварцевый песок или другой материал). Данный метод очистки применим при перманганатной окисляемости до 9.5 мгО/л. В воде обязательно присутствует двухвалентное железо, при окислении которого получается гидроксид железа, адсорбирующий и каталитически окисляющий Mn2+. Соотношение концентраций [Fe2+] / [Mn2+] меньше 7/1 быть не должно. Если в исходной водной среде такое соотношение достичь не получается, в нее добавляют сульфат железа.
Очистка воды от марганца перманганатом калия
Методика применима для поверхностных и подземных вод. При введении перманганата калия в воду растворенный марганец окисляется, в результате образуется малорастворимый оксид марганца. Осажденный оксид в виде хлопьев имеет значительную развитую удельную поверхность – около 300 м2 на 1 г осадка. Осадок – отличный катализатор, который позволяет проводить демангацию при рН около 8.5. Для удаления Mn2+ в количестве 1 мг нужно 1.92 мг перманганата калия. Как мы уже писали выше, перманганат калия убирает из воды и марганец, и железо в любых формах. Также удаляются неприятные запахи, за счет сорбционных свойств повышают вкусовые качества воды. Практические данные относительно очистки воды от марганца с применением перманганата калия показывают – нужно использовать 2 мг вещества на каждый 1 мг марганца, процент окисления будет составлять до 97%. Mn2+. После перманганата для удаления продуктов окисления, взвешенных веществ вводят коагулянт. Затем вода фильтруется на установке песчаной загрузки. При очистке подземных вод от марганца параллельно с перманганатом вводят активированную кремниевую кислоту либо флокулянты. Это позволяет увеличить хлопья оксида марганца в размерах.
Очистка воды от марганца каталитическим способом
При очистке воды от марганца и железа предварительное осаждение оксидов на поверхность зерен фильтра оказывает каталитическое воздействие на процесс окисления двухвалентного марганца кислородом (кислород используется растворенный). В процессе фильтрации предварительно аэрированной и, если это нужно, то подщелоченной воды на зернах фильтра песчаной загрузки образуется осадок гидроксида марганца Mn(OH)4. Ионы Mn2+ адсорбируются гидроксидом марганца и гидролизуются с получением Mn2O3. Последний элемент окисляется до Mn(OH)4 растворенным кислородом и снова принимает участие в каталитическом окислении. Как любой классический катализатор, элемент Mn(OH)4 практически не расходуется.
Очистка воды от марганца на модифицированной загрузке
Для увеличения рабочего ресурса фильтрующей загрузки за счет крепления пленки катализатора из оксида марганца и гидроксидов железа на поверхности зерен, для уменьшения расхода перманганата калия чаще всего используется именно модифицированная загрузка. До начала процесса фильтрования через фильтрующую загрузку пропускают сначала раствор железного купороса (FeSO4) с перманганатом калия, потом загрузку обрабатывают тринатрийфосфатом (формула Na3PO4) либо сульфитом натрия (Na2SO3). Ориентировочная скорость фильтрации воды будет составлять 8-10 м/час. Каталитическую пленку можно сделать точно так же, пропуская 0.5%-ный раствор хлорида марганца с перманганата калия через загрузку фильтра.
Очистка воды от марганца введением реагентом
Скорость окисления двухвалентного марганца хлором, диоксидом хлора, озоном либо гипохлоритом натрия зависит от показателя рН исходной воды. При введении гипохлорита натрия либо хлора эффект окисления достигается в полной мере при рН от 8.0-8.5 и времени контакта воды с окислителем один-полтора часа. В большинстве случаев обрабатываемая вода подщелачивается. Требуемая доза реагента для перевода Mn2+ в Mn4+ составляет 1.3 мг на каждый миллиграмм двухвалентного растворенного марганца. Фактические дозы будут выше.
Очистка воды от марганца диоксидом хлора или озоном
Данный тип обработки является одни из наиболее эффективных. Процесс окисления марганца занимает всего 10-15 минут при значении рН 6.5-7.0. Доза озона согласно стехиометрии составляет 1.45 мг, диоксида хлора – 1.35 мг на милиграмм двухвалентного марганца. Но поскольку озон подвергается каталитическому разложению оксидами марганца, доза должна быть увеличена. Все указанные количества KMnO4, ClO2, O3 верны, но они чисто теоретические. Практические дозы окислителей зависят от рН, срока контакта окислителя и воды отложений, содержания органических примесей и других показателей.
Очистка воды от марганца ионным обменом
Очистка воды от марганца способом ионного обмена, как и железа, происходит при водород и натрий катионировании. Методика целесообразна при необходимости глубокого умягчения, обезжелезивания и удаления марганца.
В каких случаях нужна очистка воды от железа и марганца
О высоком содержании марганца в воде свидетельствуют потеки коричнево-желтого цвета на сантехнике, желтизна на одежде, металлический привкус. Но это критерии, которые определяются на глаз, а есть еще и санитарные нормы. Они определяют предельно допустимые параметры содержания марганца в воде, даже если потеков, пятен и металлического вкуса нет, фильтрация является обязательной.
Откуда берутся железо и марганец в воде?
Железо и марганец в воду попадают из горных пород, стоков промышленных предприятий, удобрений. В природе элементы существуют в двух- и трехвалентной формах.
Фильтры для очистки воды от железа и марганца: основные материалы
Рассмотрим самые распространенные фильтрующие материалы, используемые для удаления марганца:
- Упаковки с фильтрами Birm. Устройства устанавливаются под аэраторами.
- Bewaclean – аналогичное предыдущему решение. Дополнительно данный фильтр регулирует кислотность очищаемой воды.
- Green sand – помимо марганца и железа, фильтр удаляет еще и сероводород. Для регенерации используется перманганат калия.
- МТМ – более компактный аналог Greensand с pH 6.2- 8.5.
- Pyrolox – минеральная форма марганца диоксида. Химической регенерации не требует.
Любой фильтрующий материал время от времени нужно очищать, пропуская по нему воду в обратном обычному направлению с высокой скоростью. Воду после промывки использовать в пищевых и питьевых целях нельзя.
Современные системы очистки воды для коттеджа, квартиры, дома и дачи. Варианты обустройства очистительной системы
В квартире, доме или на даче для удаления марганца удобнее всего использовать следующие системы:
- Фильтры с ионообменным картриджем.
- Фильтры обратного осмоса.
- Устройства каталитического окисления.
- Отстаиватели.
Каждый вариант имеет свои особенности, недостатки и стоимость. Перед принятием окончательного решения о выборе рекомендуем проконсультироваться со специалистами.
global-aqua.ru
Очистка воды от углекислого газа
Очистка воды от углекислого газа называется дегазацией, этот процесс бывает химическим и физическим. Во всякой природной воде всегда есть растворённые газы, причём некоторые из них оказывают коррозионное действие на трубы – такие как кислород, углекислый газ и сероводород. К тому же, последний придает воде неприятный запах тухлых яиц, а углекислый газ даже способен активно разрушать бетон. Поэтому одна из приоритетных задач – избавление от этих компонентов при очистке воды для дома или производства.
Химическая дегазация
В процессе химической очистки воды от углекислого и других газов применяются реагенты, химически связывающие газы, растворённые в ней. Например, очистить от кислорода воду можно, добавив в неё сернистый газ, сульфит натрия или гидразин.
Решения BWT для промышленной и бытовой очистки воды:
Сульфит натрия окисляется кислородом до сульфата, из сернистого газа получается вначале сернистая кислота, которая окисляется до серной. Практически полностью можно очистить воду при помощи гидразина – при реакции с ним кислород полностью поглощается, а выделяется инертный азот. Использование гидразина является наиболее эффективным способом химической очистки воды, но и самым дорогим из-за высокой стоимости реагента. Поэтому он чаще всего используется для окончательной дегазации воды после использования физических методов.
При удалении сероводорода чаще всего используется хлор, который окисляет сероводород до серы или до сульфатов. Обе реакции протекают параллельно, а преобладание одной из них зависит от рН среды и концентрации хлора.
Недостатки химических способов очистки воды от углекислого и прочих газов:
- использование реагентов удорожает и усложняет процесс очистки воды;
- передозировка реагентов приводит к ухудшению качества очищаемой воды.
Из-за этого химическая дегазация используется реже, чем физическая.
Физическая дегазация
Физически растворённые газы можно удалить из воды двумя способами:
- довести почти до нуля парциальное давление удаляемого газа в атмосфере, контактирующей с водой;
- создать условия, когда растворимость газа в воде стремится к нулю.
Первый способ называется аэрацией воды, с помощью него осуществляется очистка воды от углекислого газа и сероводорода, имеющих очень низкое парциальное давление в атмосфере.
Кислород, составляющий значительную долю атмосферы, аэрацией удалить невозможно. Поэтому для его удаления вода доводится до кипения, при котором любой газ стремится её покинуть. Вода либо нагревается в термических деаэраторах, либо её вакуумируют до момента закипания в вакуумных дегазаторах.
Существуют несколько типов дегазаторов, различающихся конструктивно, характером движения воздуха и воды и условиями процесса дегазации:
- плёночные дегазаторы. Это колонны, наполненные различными насадками, по которым тонкой плёнкой стекает вода. Насадки многократно увеличивают поверхность контакта воды с воздухом, который подаётся вентилятором во встречном направлении;
- барботажные дегазаторы. В них через толщу медленно движущейся воды проходят пузырьки сжатого воздуха;
- вакуумные дегазаторы. Здесь разрежение над водой создаётся специальными устройствами до того момента, пока она не начинает кипеть при имеющейся температуре.
В сфере водоподготовки чаще применяются плёночные дегазаторы, а для избавления от кислорода – термические или вакуумные. Дороговизна эксплуатации барботажных дегазаторов из-за большого расхода энергии на сжатие воздуха ограничивает их использование.
Проектирование дегазаторов должно отталкиваться от следующих параметров:
- площадь поперечного сечения аппарата, которая зависит от допустимой плотности орошения насадки;
- площадь поверхности насадки, необходимой для эффективной дегазации;
- расход воздуха.
Очистка воды от углекислого газа, кислорода и сероводорода – важный этап комплексной водоочистки. Эта процедура позволяет избавиться от вредных компонентов, которые в противном случае оказывают губительное воздействие на дорогостоящее промышленное оборудование.
Смотрите также:
www.bwt.ru